Dielétricos polares e apolares
De acordo com as visões da física clássica, os dielétricos são fundamentalmente diferentes dos condutores, porque em condições normais não há cargas elétricas livres neles. A carga total das partículas que formam moléculas dielétricas é zero. No entanto, isso não significa de forma alguma que as moléculas dessas substâncias não sejam capazes de exibir propriedades elétricas.
Todos os dielétricos lineares conhecidos podem ser divididos em dois grandes grupos: dielétricos polares e dielétricos apolares. Essa divisão é introduzida devido às diferenças nos mecanismos de polarização das moléculas de cada tipo de dielétrico. De facto, o mecanismo de polarização revela-se um aspecto extremamente importante quer no estudo das propriedades físicas e químicas dos dieléctricos, quer no estudo das suas propriedades eléctricas.
Dielétricos apolares
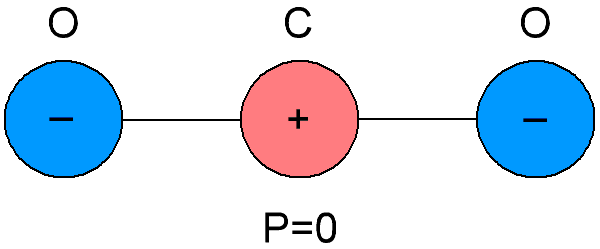
Os dielétricos apolares também são chamados de dielétricos neutros, porque as moléculas das quais esses dielétricos são compostos diferem na coincidência dos centros de gravidade das cargas negativas e positivas dentro deles.Como resultado, verifica-se que as moléculas de dielétricos apolares não possuem momento elétrico próprio, é igual a zero. E na ausência de um campo elétrico externo, as cargas positivas e negativas das moléculas dessas substâncias são dispostas simetricamente.
Se um campo elétrico externo for aplicado a um dielétrico apolar, então as cargas positiva e negativa nas moléculas serão deslocadas de sua posição de equilíbrio original, as moléculas se tornarão dipolos cujos momentos elétricos serão agora proporcionais à força da força elétrica. campo aplicado a eles, e será direcionado paralelamente ao campo.
Exemplos de dielétricos apolares que são usados com sucesso hoje como materiais isolantes elétricos são os seguintes: polietileno, poliestireno, hidrocarbonetos, óleos isolantes de petróleo, etc. Além disso, representantes brilhantes de moléculas apolares são, por exemplo, nitrogênio, dióxido de carbono, metano, etc. Senhor.
Os dielétricos apolares, por causa de seus valores tangentes de baixa perda dielétrica, são amplamente usados como dielétricos de alta frequência em capacitores como o K78-2.
Dielétricos polares
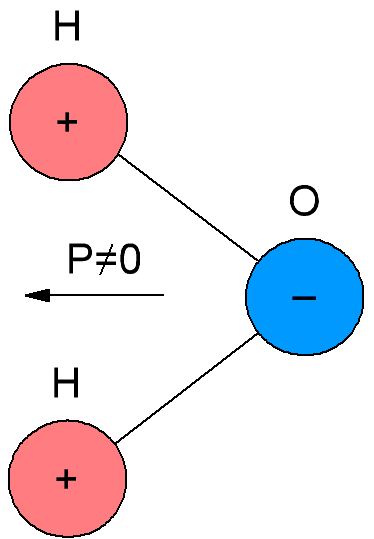
Nos dielétricos polares, também chamados de dielétricos dipolo, as moléculas possuem seu próprio momento elétrico, ou seja, suas moléculas são polares. A razão é que as moléculas de dielétricos polares têm uma estrutura assimétrica, de modo que os centros de massa de cargas negativas e positivas nas moléculas de tais dielétricos não coincidem.
Se em um polímero apolar alguns dos átomos de hidrogênio forem substituídos por átomos de outros elementos ou por radicais não hidrocarbonetos, obteremos apenas um dielétrico polar (dipolo), pois a simetria será quebrada como resultado de tal substituição. Determinando a polaridade de uma substância por sua fórmula química, o pesquisador deve, é claro, ter uma ideia da estrutura espacial de suas moléculas.
Quando não há campo elétrico externo, os eixos dos dipolos moleculares são orientados arbitrariamente devido ao movimento térmico, de modo que na superfície do dielétrico e em cada elemento de seu volume a carga elétrica é em média zero. No entanto, quando um dielétrico é introduzido em um campo externo, ocorre uma orientação parcial dos dipolos moleculares.Como resultado, cargas não compensadas macroscopicamente conectadas aparecem na superfície do dielétrico, criando um campo direcionado para o campo externo.
Exemplos de dielétricos polares incluem os seguintes: hidrocarbonetos clorados, resinas epóxi e fenol formaldeído, compostos de silício silício, etc. Moléculas de água e álcool, por exemplo, também são exemplos notáveis de moléculas polares. Os dielétricos polares são amplamente utilizados em vários campos da tecnologia, como piezoelétrico e ferroelétrico, óptica, óptica não linear, eletrônica, acústica, etc.

