Como as baterias funcionam e funcionam
 No sentido mais amplo da palavra em tecnologia, o termo "bateria" refere-se a um dispositivo que permite, sob certas condições de operação, acumular um determinado tipo de energia e, em outras, usá-lo para as necessidades humanas.
No sentido mais amplo da palavra em tecnologia, o termo "bateria" refere-se a um dispositivo que permite, sob certas condições de operação, acumular um determinado tipo de energia e, em outras, usá-lo para as necessidades humanas.
Eles são usados onde é necessário coletar energia por um certo tempo e depois usá-la para realizar grandes processos de trabalho intensivo. Por exemplo, acumuladores hidráulicos usados em eclusas permitem que os navios subam a um novo nível no leito do rio.
As baterias elétricas funcionam com eletricidade de acordo com o mesmo princípio: primeiro, elas acumulam (acumulam) eletricidade de uma fonte de carregamento externa e depois a fornecem aos consumidores conectados para que funcionem. Pela sua natureza, pertencem a fontes químicas de corrente capazes de realizar ciclos periódicos de descarga e carga repetidamente.
Durante a operação, ocorrem constantemente reações químicas entre os componentes das placas do eletrodo com sua substância de enchimento - eletrólito.
Um diagrama esquemático de um dispositivo de bateria pode ser representado por um desenho simplificado quando duas placas de metais diferentes com fios são inseridas no corpo da embarcação para fornecer contatos elétricos. Um eletrólito é derramado entre as placas.
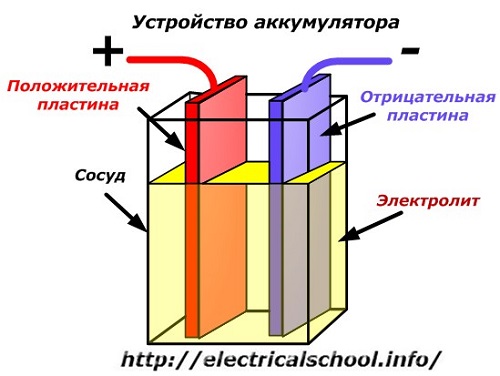
Funcionamento da bateria quando descarregada
Quando uma carga, como uma lâmpada, é conectada aos eletrodos, um circuito elétrico fechado é criado através do qual a corrente de descarga flui. É formado pelo movimento de elétrons em peças metálicas e ânions com cátions no eletrólito.
Este processo é convencionalmente mostrado em um diagrama com um design de eletrodo de níquel-cádmio.
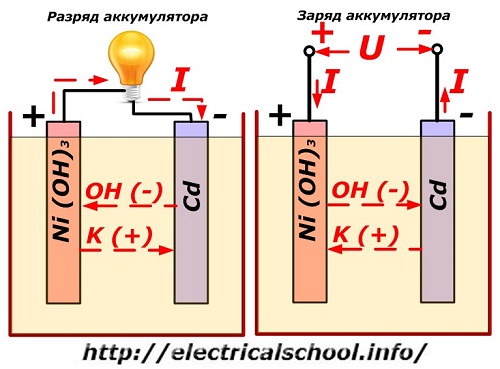
Aqui, óxidos de níquel com aditivos de grafite, que aumentam a condutividade elétrica, são usados como material do eletrodo positivo. O metal do eletrodo negativo é cádmio esponjoso.
Durante a descarga, as partículas de oxigênio ativo dos óxidos de níquel são liberadas no eletrólito e direcionadas para as placas negativas, onde o cádmio é oxidado.
Desempenho da bateria ao carregar
Quando a carga é desligada, uma tensão constante (em certas situações, pulsante) é aplicada aos terminais da placa de valor maior que o de uma bateria carregada de mesma polaridade, quando os terminais positivo e negativo da fonte e do consumidor coincidem .
O carregador sempre tem mais potência, o que “suprime” a energia residual na bateria e cria uma corrente elétrica no sentido contrário ao da descarga. Como resultado, os processos químicos internos entre os eletrodos e o eletrólito mudam. Por exemplo, em uma caixa de placas de níquel-cádmio, o eletrodo positivo é enriquecido com oxigênio e o negativo - para um estado de cádmio puro.
Quando a bateria é descarregada e carregada, a composição química do material das placas (eletrodos) muda, mas o eletrólito não muda.
Métodos de conexão da bateria
conexão paralela
A quantidade de corrente de descarga que uma pessoa pode suportar depende de muitos fatores, mas principalmente do projeto, materiais usados e suas dimensões. Quanto maior a área das placas nos eletrodos, maior a corrente que elas podem suportar.
Este princípio é usado para conectar células do mesmo tipo em paralelo em baterias quando é necessário aumentar a corrente para a carga, mas para carregar tal projeto, será necessário aumentar a potência da fonte. Este método raramente é usado para estruturas prontas, pois agora é muito mais fácil comprar imediatamente a bateria necessária. Mas os fabricantes de baterias ácidas o usam, conectando diferentes placas em blocos únicos.
conexão serial
Dependendo dos materiais utilizados, uma tensão de 1,2 / 1,5 ou 2,0 volts pode ser gerada entre as duas placas de eletrodos de baterias comuns no dia a dia. (Na verdade, esse intervalo é muito mais amplo.) Obviamente, não é suficiente para muitos dispositivos elétricos. Portanto, baterias do mesmo tipo são conectadas em série, e isso geralmente é feito em um caso.
Um exemplo de tal projeto é o amplo desenvolvimento automotivo baseado em ácido sulfúrico e placas de eletrodo de chumbo.
Normalmente, entre as pessoas, especialmente entre os motoristas de transporte, costuma-se chamar qualquer dispositivo de bateria, independentemente do número de seus elementos constituintes - caixas. No entanto, isso não é totalmente correto.A estrutura, montada a partir de várias caixas ligadas em série, já é uma bateria, à qual está afixada a abreviatura «АКБ»... A sua estrutura interna é apresentada na figura.
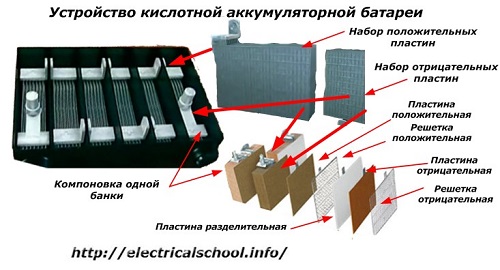
Cada um dos frascos consiste em dois blocos com um conjunto de placas para os eletrodos positivo e negativo. Os blocos se encaixam sem contato metálico com a possibilidade de uma conexão galvânica confiável através do eletrólito.
Neste caso, as placas de contato possuem uma grade adicional e são separadas umas das outras por uma placa separadora.
Conectar as placas em blocos aumenta sua área de trabalho, reduz a resistência total de toda a estrutura e permite aumentar a potência da carga conectada.
Na parte externa da caixa, essa bateria possui os elementos mostrados na figura abaixo.
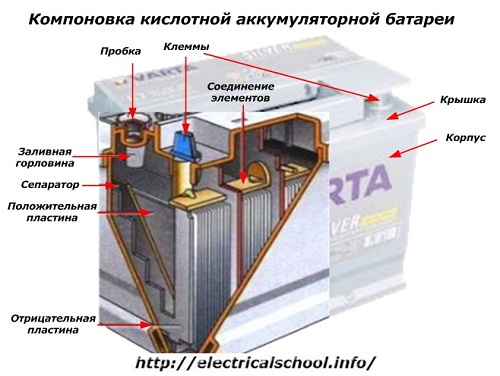
Ele mostra que a caixa de plástico resistente é selada com uma tampa e equipada com dois terminais (geralmente em forma de cone) na parte superior para conexão com o circuito elétrico do carro. Marcas de polaridade estão estampadas em seus terminais: «+» e «-«. Normalmente, o terminal positivo tem um diâmetro ligeiramente maior que o terminal negativo para bloquear erros de fiação.
As baterias reparáveis têm um orifício de enchimento na parte superior de cada frasco para controlar o nível de eletrólito ou adicionar água destilada durante a operação. Um plugue é aparafusado nele, o que protege as cavidades internas da caixa contra contaminação e ao mesmo tempo evita que o eletrólito derrame quando a bateria é inclinada.
Como com uma carga potente, é possível gaseificar do eletrólito (e esse processo é possível durante a condução intensiva), são feitos furos nos plugues para evitar que a pressão dentro da caixa aumente.Oxigênio e hidrogênio, bem como vapores de eletrólitos, saem por eles. Recomenda-se evitar tais situações envolvendo correntes de carga excessivas.
A mesma figura mostra a conexão dos elementos entre os bancos e a disposição das placas dos eletrodos.
As baterias de arranque para automóveis (chumbo-ácido) funcionam segundo o princípio da dupla sulfatação. Durante a descarga/carga, ocorre sobre eles um processo eletroquímico, acompanhado de alteração na composição química da massa ativa dos eletrodos com liberação/absorção de água no eletrólito (ácido sulfúrico).
Isso explica o aumento da gravidade específica do eletrólito durante o carregamento e a diminuição quando a bateria é descarregada. Em outras palavras, o valor da densidade permite avaliar a condição elétrica da bateria. Um dispositivo especial é usado para medi-lo - um hidrômetro de carro.
A água destilada, que faz parte do eletrólito das baterias ácidas, transforma-se em estado sólido - gelo em temperaturas negativas. Portanto, para evitar que as baterias dos carros congelem no frio, é necessário aplicar medidas especiais previstas nas regras para exploração.
Que tipos de baterias existem?
A produção moderna para diversos fins produz mais de três dezenas de produtos com diferentes composições de eletrodos e eletrólitos. 12 modelos conhecidos funcionam apenas com lítio.

O seguinte pode ser encontrado como metal de eletrodo:
-
liderar;
-
ferro;
-
lítio;
-
titânio;
-
cobalto;
-
cádmio;
-
níquel;
-
zinco;
-
prata;
-
vanádio;
-
alumínio
-
alguns outros itens.
Eles afetam as características de saída elétrica e, portanto, a aplicação.
A capacidade de suportar altas cargas de curto prazo resultantes da rotação dos virabrequins dos motores de combustão interna por motores elétricos de partida é característica das baterias de chumbo-ácido. Eles são amplamente utilizados em transporte, fontes de alimentação ininterruptas e sistemas de energia de emergência.
Padrão células galvânicas (baterias comuns) são geralmente substituídas por baterias de níquel-cádmio, níquel-zinco e níquel-hidreto metálico.
Mas os projetos de íon de lítio ou polímero de lítio funcionam de forma confiável em dispositivos móveis e de computação, ferramentas de construção e até veículos elétricos.
De acordo com o tipo de eletrólito utilizado, as baterias são:
-
azedo
-
alcalino.
Existe uma classificação das baterias de acordo com a finalidade. Por exemplo, nas condições modernas, surgiram dispositivos usados \u200b\u200bpara transferência de energia - recarga de outras fontes. A chamada bateria externa ajuda os proprietários de muitos dispositivos móveis na ausência de uma rede elétrica alternada. É capaz de carregar repetidamente um tablet, smartphone, telefone celular.
Todas essas baterias têm o mesmo princípio de operação e um dispositivo semelhante. Por exemplo, o modelo de dedo de íon-lítio mostrado na figura abaixo repete de muitas maneiras o projeto das baterias ácidas discutidas anteriormente.
Aqui vemos os mesmos eletrodos de contato, placas, separador e carcaça. Só eles são feitos levando em consideração outras condições de trabalho.
Características elétricas básicas de uma bateria
A operação do dispositivo é afetada pelos parâmetros:
-
capacidade;
-
densidade de energia;
-
auto descarga;
-
regime de temperatura.
A capacidade é chamada de carga máxima da bateria, que é capaz de fornecer durante a descarga para a tensão mais baixa. É expresso em pendentes (sistema SI) e ampères-hora (unidade não pertencente ao sistema).
Como tipo de capacidade existe a «capacidade energética», que determina a energia libertada durante a descarga à tensão mínima admissível. É medido em joules (SI) e watt-hora (unidades não SI).
Densidade de energia expressa como a razão entre a quantidade de energia e o peso ou volume da bateria.
A autodescarga considera a perda de capacidade após o carregamento na ausência de carga nos terminais. Isso depende do projeto e é exacerbado por falhas de isolamento entre os eletrodos por vários motivos.
A temperatura de operação afeta as propriedades elétricas e, em caso de desvios graves da norma especificada pelo fabricante, pode danificar a bateria. Calor e frio são inaceitáveis, pois afetam o curso das reações químicas e a pressão do ambiente dentro da caixa.
