Corrente elétrica em líquidos e gases
Corrente elétrica em líquidos
 Em um condutor de metal eletricidade é formado pelo movimento direcionado de elétrons livres e que nenhuma mudança ocorra na substância da qual o condutor é feito.
Em um condutor de metal eletricidade é formado pelo movimento direcionado de elétrons livres e que nenhuma mudança ocorra na substância da qual o condutor é feito.
Esses condutores, nos quais a passagem da corrente elétrica não é acompanhada por mudanças químicas em sua substância, são chamados condutores de primeira classe... Eles incluem todos os metais, carvão e várias outras substâncias.
Mas na natureza também existem condutores de corrente elétrica nos quais ocorrem fenômenos químicos durante a passagem da corrente. Esses condutores são chamados de condutores de segundo tipo... Eles incluem principalmente várias soluções em água de ácidos, sais e bases.
Se você derramar água em um recipiente de vidro e adicionar algumas gotas de ácido sulfúrico (ou algum outro ácido ou álcali), e então pegar duas placas de metal e prender fios a elas, abaixando essas placas no recipiente e conectar uma corrente fonte para as outras pontas dos fios através da chave e do amperímetro, então o gás será liberado da solução e continuará continuamente enquanto o circuito estiver fechado.a água acidificada é de fato um condutor. Além disso, as placas começarão a ficar cobertas de bolhas de gás. Então essas bolhas vão se desprender das placas e sair.
Quando uma corrente elétrica é passada através da solução, ocorrem mudanças químicas, resultando na liberação de um gás.
Eles são chamados de condutores do segundo tipo de eletrólitos, e o fenômeno que ocorre no eletrólito quando uma corrente elétrica passa por ele é a eletrólise.
Placas de metal imersas em um eletrólito são chamadas de eletrodos; um deles ligado ao pólo positivo da fonte de corrente é chamado de ânodo e o outro ligado ao pólo negativo é o cátodo.
O que determina a passagem da corrente elétrica em um líquido condutor? Acontece que nessas soluções (eletrólitos) as moléculas de ácido (álcalis, sal) sob a ação de um solvente (neste caso a água) se dividem em dois componentes e uma parte da molécula tem uma carga elétrica positiva e a outra uma um negativo.
As partículas de uma molécula que possuem carga elétrica são chamadas de íons... Quando um ácido, sal ou álcali é dissolvido em água, um grande número de íons positivos e negativos ocorre na solução.
Agora deve ficar claro por que uma corrente elétrica passou pela solução, porque entre os eletrodos conectados à fonte de corrente, um diferença potencialem outras palavras, um deles acabou sendo carregado positivamente e o outro carregado negativamente. Sob a influência dessa diferença de potencial, os íons positivos começaram a se misturar em direção ao eletrodo negativo - o cátodo e os íons negativos - em direção ao ânodo.
Assim, o movimento caótico dos íons tornou-se um movimento oposto ordenado de íons negativos em uma direção e íons positivos na outra.Esse processo de transferência de carga é um fluxo de corrente elétrica através do eletrólito e ocorre enquanto houver uma diferença de potencial entre os eletrodos. À medida que a diferença de potencial desaparece, a corrente através do eletrólito para, o movimento ordenado dos íons é interrompido e o movimento caótico começa novamente.
Como exemplo, considere o fenômeno da eletrólise, quando uma corrente elétrica passa por uma solução de sulfato de cobre CuSO4 com eletrodos de cobre abaixados nela.
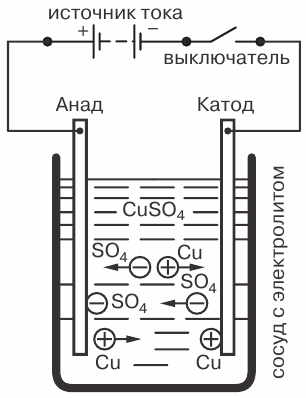
O fenômeno da eletrólise quando a corrente passa por uma solução de sulfato de cobre: C — recipiente com eletrólito, B — fonte de corrente, C — interruptor
Haverá também um movimento reverso de íons para os eletrodos. O íon positivo será o íon cobre (Cu) e o íon negativo será o resíduo ácido (SO4). Os íons de cobre, quando em contato com o cátodo, serão descarregados (juntando os elétrons que faltam a si), ou seja, serão convertidos em moléculas neutras de cobre puro e serão depositados no cátodo na forma de partículas mais finas (moleculares). ) camada.
Os íons negativos que atingem o ânodo também são ejetados (doam elétrons em excesso). Mas, ao mesmo tempo, eles entram em uma reação química com o cobre do ânodo, como resultado da qual uma molécula de cobre Cti é adicionada ao resíduo ácido SO4, e uma molécula de sulfato de cobre CnasO4 é formada e devolvida ao eletrólito.
Como esse processo químico leva muito tempo, o cobre é depositado no cátodo, que é liberado do eletrólito. Nesse caso, o eletrólito, ao invés das moléculas de cobre que iam para o cátodo, recebe novas moléculas de cobre devido à dissolução do segundo eletrodo, o ânodo.
O mesmo processo ocorre se eletrodos de zinco forem usados em vez de cobre, e o eletrólito for uma solução de sulfato de zinco ZnSO4.O zinco também será transferido do ânodo para o cátodo.
Portanto, uma diferença entre corrente elétrica em metais e condutores líquidos reside no fato de que nos metais os portadores de carga são apenas elétrons livres, ou seja, cargas negativas enquanto em eletrólitos eletricidade carregados por partículas de matéria com cargas opostas — íons movendo-se em direções opostas. É por isso que se diz que os eletrólitos têm condutividade iônica.

O fenômeno da eletrólise foi descoberto em 1837 por B. S. Jacobi, que fez inúmeras experiências para estudar e melhorar as fontes químicas de corrente. Jacobi descobriu que um dos eletrodos colocados em uma solução de sulfato de cobre, quando uma corrente elétrica passava por ele, era revestido de cobre.
Esse fenômeno é chamado de eletroformação, agora encontra uma aplicação prática extremamente grande. Um exemplo disso é o revestimento de objetos metálicos com uma fina camada de outros metais, por exemplo, niquelagem, folheação a ouro, prata, etc.
Corrente elétrica em gases
Os gases (incluindo o ar) não conduzem eletricidade em condições normais. Por exemplo, uma meta fios para linhas aéreassendo suspensos paralelamente um ao outro, eles são isolados um do outro por uma camada de ar.
Porém, sob a influência de altas temperaturas, grande diferença de potencial e outros motivos, gases, como condutores líquidos, ionizam, ou seja, partículas de moléculas de gás aparecem neles em grande número, que, como portadores de eletricidade, contribuem para a passagem de uma corrente elétrica através do gás.
Mas, ao mesmo tempo, a ionização de um gás difere da ionização de um líquido condutor.Se a molécula se divide em duas partes carregadas em um líquido, então, em gases sob a ação da ionização, os elétrons são sempre separados de cada molécula e o íon permanece na forma de uma parte carregada positivamente da molécula.
Basta interromper a ionização do gás, pois ele deixa de ser condutor, enquanto o líquido permanece sempre condutor de corrente elétrica. Portanto, a condutividade do gás é um fenômeno temporário, dependendo da ação de causas externas.

No entanto, há algo mais tipo de descarga elétricaChamado de descarga de arco ou simplesmente arco elétrico. O fenômeno do arco elétrico foi descoberto no início do século 19 pelo primeiro engenheiro elétrico russo V. V. Petrov.
V.V. Realizando inúmeros experimentos, Petrov descobriu que entre dois carvões conectados a uma fonte de corrente, uma descarga elétrica contínua aparecia no ar, acompanhada de uma luz brilhante. Em seus escritos, V.V. Petrov escreveu que, neste caso, "a calma escura pode ser suficientemente iluminada". Assim, pela primeira vez, foi obtida luz elétrica, que foi praticamente aplicada por outro engenheiro elétrico russo, Pavel Nikolayevich Yablochkov.
"Svesht Yablochkov", cujo trabalho é baseado no uso de um arco elétrico, fez uma verdadeira revolução na engenharia elétrica da época.

A descarga de arco é hoje usada como fonte de luz, por exemplo, em holofotes e dispositivos de projeção. A alta temperatura da descarga do arco permite que seja utilizado para dispositivos de forno de arco… Atualmente, os fornos a arco acionados por corrente muito alta são usados em várias indústrias: para fusão de aço, ferro fundido, ferroligas, bronze, etc. E em 1882, NN Benardos usou pela primeira vez a descarga de arco para cortar e soldar metais.
Em tubos de gás, lâmpadas fluorescentes, estabilizadores de tensão, para obter feixes de elétrons e íons, a chamada descarga de gás incandescente.
Descarga de centelha Usado para medir grandes diferenças de potencial usando um centelhador esférico, cujos eletrodos são duas esferas de metal com superfície polida. As bolas são afastadas e uma diferença de potencial mensurável é aplicada a elas. As bolas são então aproximadas até que uma faísca passe entre elas. Conhecendo o diâmetro das esferas, a distância entre elas, a pressão, a temperatura e a umidade do ar, encontram a diferença de potencial entre as esferas conforme tabelas especiais. Com este método é possível medir com uma precisão de alguns por cento uma diferença de potencial da ordem de dezenas de milhares de volts.
